A Peptidek Túlélési Kémiája: Enzimatikus Gátak és a Molekuláris Tuning Tudománya
A bőrünk korántsem egy steril, passzív felület, sokkal inkább egy aktív biológiai harctér. Ahogy azt Meyer-Hoffert (2015) kutatásai az antimikrobiális peptidek kapcsán részletezik, afelszíni mikrobiom zónájában és azélő hámrétegben (epidermis) proteáz és peptidáz enzimek valóságos hadserege járőrözik. Különösen a Kallikrein-típusú peptidázok (KLKs) és a Mátrix Metalloproteinázok (MMP-k) dominálnak ezen a területen. Bár ezek az enzimek…
A bőrünk korántsem egy steril, passzív felület, sokkal inkább egy aktív biológiai harctér. Ahogy azt Meyer-Hoffert (2015) kutatásai az antimikrobiális peptidek kapcsán részletezik, afelszíni mikrobiom zónájában és azélő hámrétegben (epidermis) proteáz és peptidáz enzimek valóságos hadserege járőrözik. Különösen a Kallikrein-típusú peptidázok (KLKs) és a Mátrix Metalloproteinázok (MMP-k) dominálnak ezen a területen. Bár ezek az enzimek alapvetően a bőr természetes védekező és megújulási folyamatainak, például a szabályozott hámlasztásnak (deszkvamáció) a nélkülözhetetlen szabályozói, egy külső hatóanyag szempontjából kíméletlen kapuőrökként viselkednek.
A probléma drámai, és a biohasznosulás szempontjából kulcsfontosságú: amint ezek az enzimek felismernek egy szabad, védelem nélküli aminosav-láncot, vagyis egy úgynevezett „meztelen” peptidet, a szubsztrát-specifikus lebontás azonnal megindul.
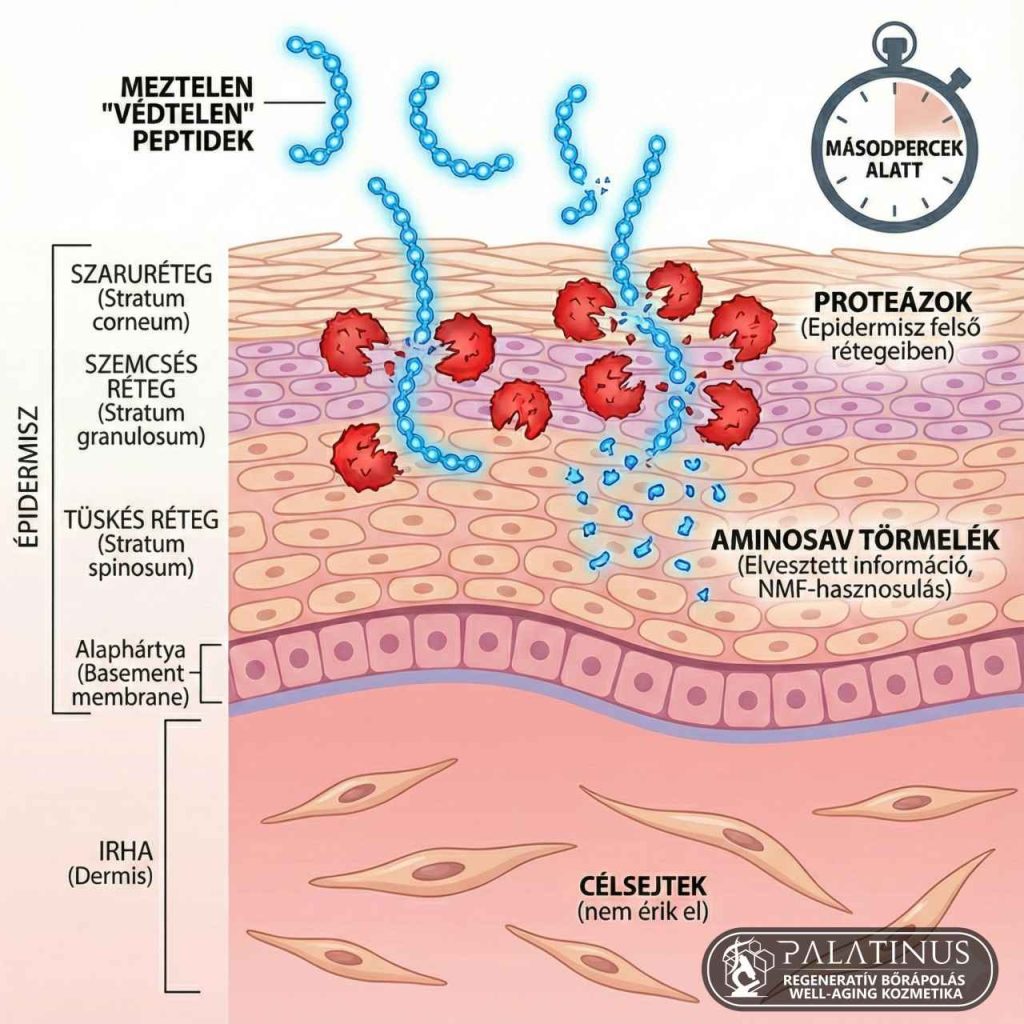
A szakmai realitás kijózanító, ugyanis egy ilyen módosítatlan peptid biológiai felezési ideje a bőr aktív rétegeiben gyakran nem percekben, hanem csupán másodpercekben mérhető (Lupo & Cole, 2007). Mielőtt a molekula egyáltalán esélyt kapna arra, hogy a passzív diffúzió révén elérje a célsejteket, például a mélyebben fekvő fibroblasztokat, az enzim-környezet hidrolizálja, azaz szétvágja a peptidkötéseket. A drága hatóanyagból ilyenkor nem marad más, mint egyszerű aminosav-törmelék, amely bár tápláléknak és humektánsnak (NMF-pótlásnak) kiváló a sejtek számára, a remélt sejtkommunikációs és ránctalanító funkció betöltésére, a specifikus térszerkezet (bioaktív konformáció) elvesztése miatt már teljesen alkalmatlan.
Ennek a biokémiai kihívásnak a megoldására a modern biotechnológia a kémiai módosítás, vagyis a „molekuláris tuning” eszközéhez nyúlt, mintegy láthatatlan páncéllal vértezve fel a sérülékeny hatóanyagokat. Az első védelmi stratégia a molekula végeit célozza. Mivel minden peptid rendelkezik egy szabad N-terminális elejével és egy C-terminális véggel, a bőrbontó enzimek nagy része, az úgynevezett exopeptidázok (különösen az aminopeptidázok), előszeretettel kezdik meg a lebontást éppen ezeken a pontokon. Ezt a támadási felületet a vegyészek úgy iktatják ki, hogy a lánc elejére egy kémiai csoportot, leggyakrabban ecetsavat illesztenek, amit acetilálásnak nevezünk.
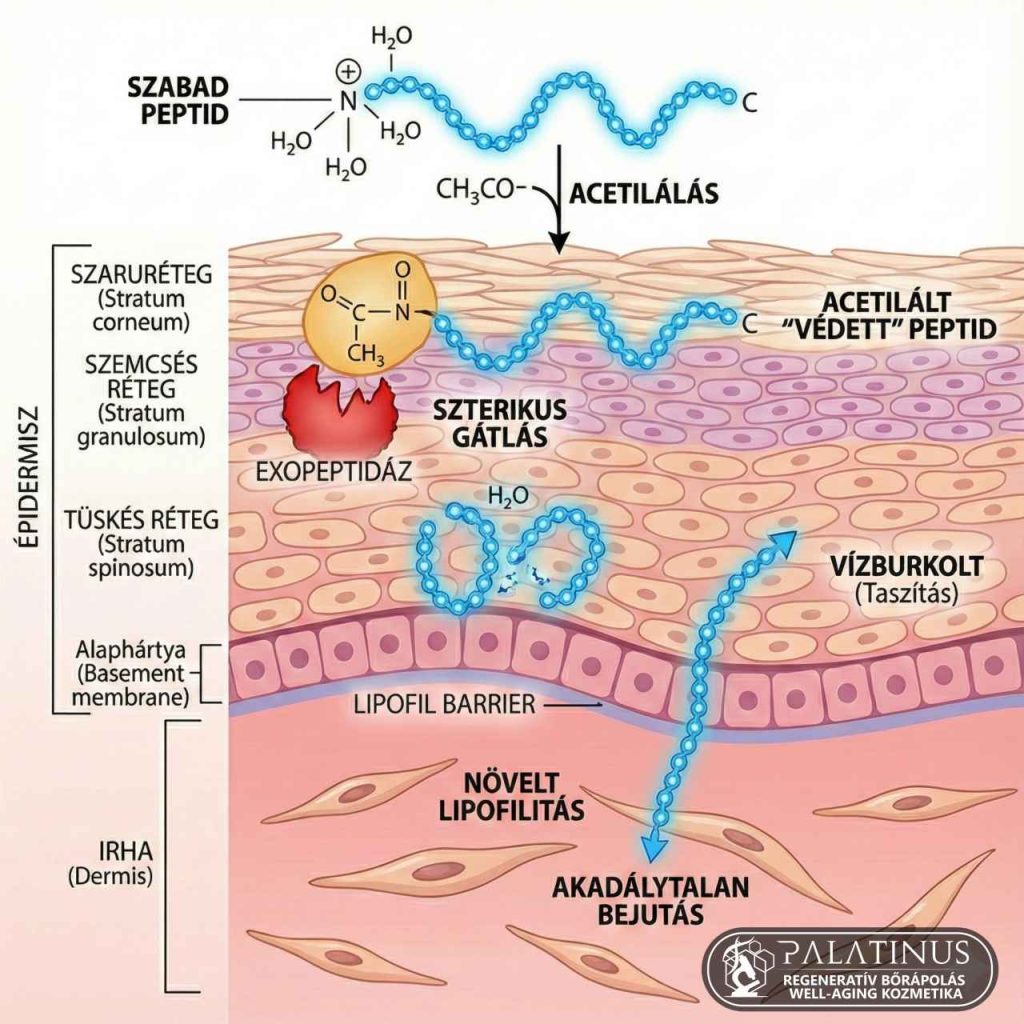
Ez a látszólag apró módosítás kettős védelmet biztosít. Egyrészt érvényesül a szterikus gátlás elve, amikor az újonnan felhelyezett csoport megváltoztatja a molekula térbeli szerkezetét, így az enzim „ollója” fizikailag nem fér hozzá a hasítási ponthoz. Másrészt, és biofizikai szempontból talán ez a fontosabb tényező, megtörténik a töltés semlegesítés. A peptidek szabad végei ugyanis fiziológiás pH-n pozitív elektromos töltéssel rendelkeznek, ami hidrátburkot (vizet) vonz a molekula köré. Márpedig a Bos és Meinardi (2000) által definiált 500 Daltonos szabály egyik kitétele, hogy a bőr zsíros barrierje taszítja az ionos, vízburkolt anyagokat. Az acetilálás semlegesíti ezt a töltést, így a molekula elveszíti „vizes burkát”, növekszik a lipofilitása, és képes akadálytalanul besimulni a bőr lipofil közegébe.
A védekezés másik, talán még rafináltabb szintje a „Trójai faló” módszere, amely a legismertebb peptidek, például a Matrixyl (Palmitoyl Pentapeptide-4) hatékonyságának is az alapja. Ebben az esetben a vízoldékony peptidhez kovalens kötéssel egy hosszú szénláncú zsírsavat, például palmitinsavat kapcsolnak. Ez a technológia, amelyet Lintner és Peschard (2000) úttörő munkássága alapozott meg, a „hasonlót a hasonlóval” elvre épít: mivel a bőr külső védőrétege, a stratum corneum szerkezetileg egy téglafalhoz hasonlít, ahol a habarcs egy kemény lipidréteg, a vizes bázisú anyagok egyszerűen lepattannának róla.
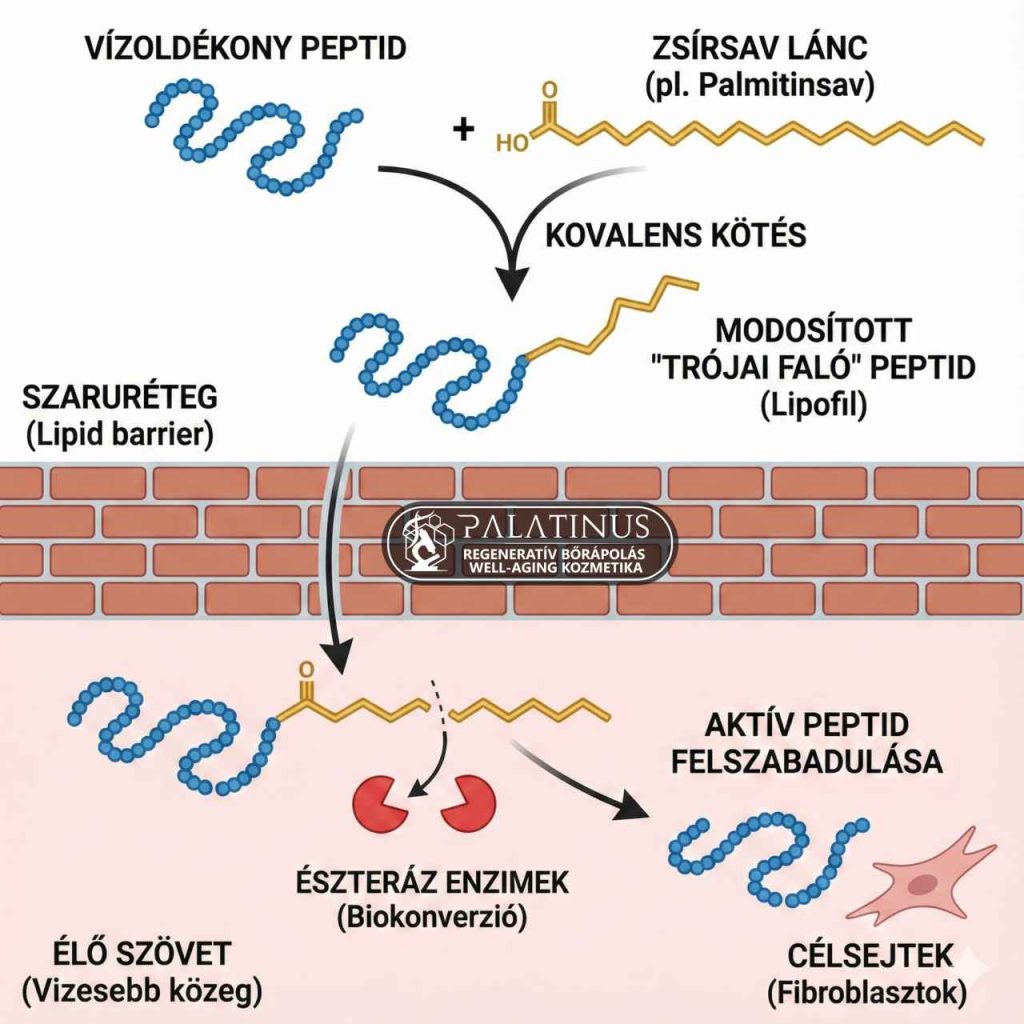
Ám amint a peptid megkapja ezt a „zsíros farkincát”, a kémiai karaktere megváltozik, és lipofillé, azaz zsírkedvelővé válik. Ez a zsíros lánc már képes feloldódni a bőr barrier-lipidjeiben, és magával húzza a peptid-láncot a mélyebb rétegek felé.
A folyamat zsenialitása a gyógyszerészetből átvett „prodrug” (előgyógyszer) mechanizmusban rejlik: a koncepció szerint miután a molekula sikeresen átjutott a barrieren és bekerült az élő szövet vizesebb közegébe, a bőrben jelenlévő nem-specifikus észteráz enzimek biokonverzió révén lehasítják a segítő zsírsavat, mint egy űrhajóról leváló hordozórakétát. Így végül felszabadul az aktív, tiszta peptid, pontosan ott és pontosan akkor, amikor a receptornak szüksége van rá, maximalizálva ezzel a lokális biohasznosulást.
A folytatásban a A Peptidek Bioaktivitás Illúzióját: Proteolitikus Gátak és az In Vitro Csapda jelenségét járjuk körbe.