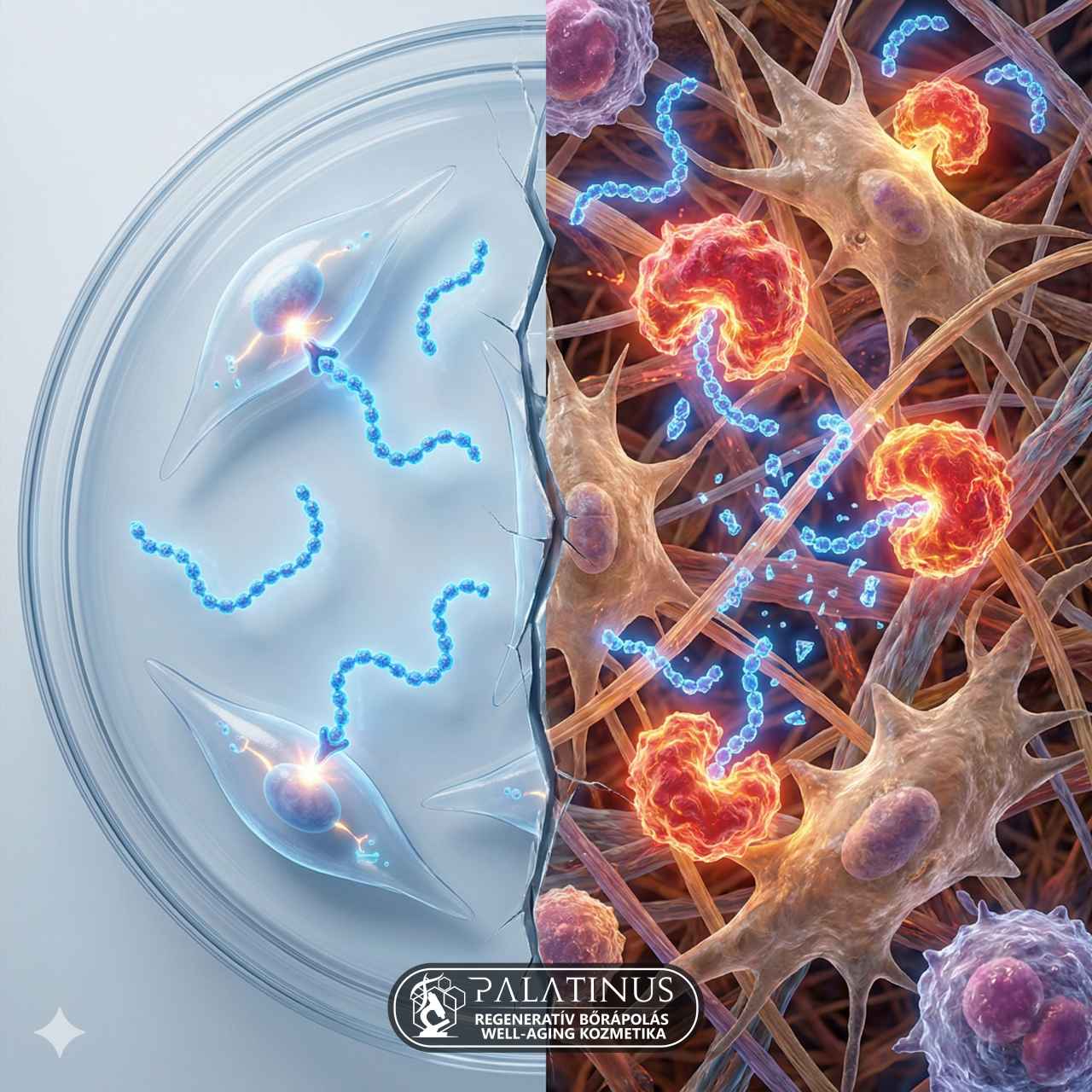
A Peptidek Bioaktivitás Illúziója: Proteolitikus Gátak és az In Vitro Csapda
A modern kozmetológia egyik legsúlyosabb, gyakran elhallgatott dilemmája a laboratóriumi eredmények és a valós klinikai hatékonyság közötti tátongó szakadék. Amikor a peptid-alapú hatóanyagok biológiai sorsát vizsgáljuk, le kell számolnunk azzal a romantikus elképzeléssel, hogy a bőr egy passzív, szivacsszerű felszívó közeg. A valóságban a bőrünk egy aktív, immunológiailag kompetens szerv, amelynek elsődleges feladata a „non-self”…
A modern kozmetológia egyik legsúlyosabb, gyakran elhallgatott dilemmája a laboratóriumi eredmények és a valós klinikai hatékonyság közötti tátongó szakadék. Amikor a peptid-alapú hatóanyagok biológiai sorsát vizsgáljuk, le kell számolnunk azzal a romantikus elképzeléssel, hogy a bőr egy passzív, szivacsszerű felszívó közeg. A valóságban a bőrünk egy aktív, immunológiailag kompetens szerv, amelynek elsődleges feladata a „non-self” (nem saját) anyagok detektálása és semlegesítése. Ebben a biológiai kereszttűzben a védelem nélküli, úgynevezett „meztelen” peptidek sorsa determinisztikus: a hatóanyag-bevitel nem egyszerű transzportfolyamat, hanem versenyfutás az idővel és a bőr metabolikus barrierjével.
A szakirodalomban gyakran emlegetett „120 másodperces halálos ítélet” nem költői túlzás, hanem a kután proteázok és peptidázok aktivitásának kinetikai realitása.
Ahogy azt Meyer-Hoffert (2015) kutatásai is részletezik, a bőr felszínén, a mikrobiom flórájában és az epidermisz extracelluláris terében jelenlévő enzimrendszerek, különösen a Kallikrein-típusú peptidázok (KLKs), a szerin-proteázok és a Mátrix Metalloproteinázok (MMP-k), evolúciósan arra lettek tervezve, hogy a sérült vagy idegen fehérjeláncokat aminosavakra bontsák.
Ez a proteolitikus kaszkád a barrier integritásának védelmét szolgálja a potenciális kórokozókkal szemben. Amikor egy védelem nélküli, lineáris peptidlánc érintkezik ezzel a közeggel, a peptidkötések hidrolízise szinte azonnal megindul. A farmakokinetikai felezési idő drámai lerövidülése azt eredményezi, hogy mire a molekula a passzív diffúzió lassú folyamatával átjutna a stratum corneum lipidmátrixán, a degradáció mértéke kritikussá válik (Namjoshi & Benson, 2010).
Ez a bomlás a bioaktivitás végét jelenti. A peptid-receptor kölcsönhatás ugyanis a szigorú „kulcs a zárba” elv alapján működik: ha a peptid lánca elszakad, vagy elveszíti specifikus térbeli konformációját, a molekula többé nem képes beilleszkedni a célsejt (pl. fibroblaszt) receptorába. Ami a bőrfelszínre még ígéretes szignálmolekulaként érkezett, az percek alatt egyszerű aminosav-törmelékké degradálódik. Bár ezek a szabaddá vált aminosavak, mint a bőr természetes hidratáló faktorának (NMF) építőelemei, kiváló humektáns (vízmegkötő) hatással bírnak, információhordozó képességük megszűnik. A sejtkommunikációs parancs, legyen az „termelj kollagént” vagy „lazítsd el az izmot”, sosem ér célba, a biológiai levél elveszik a postán, mielőtt a címzett elolvashatná.
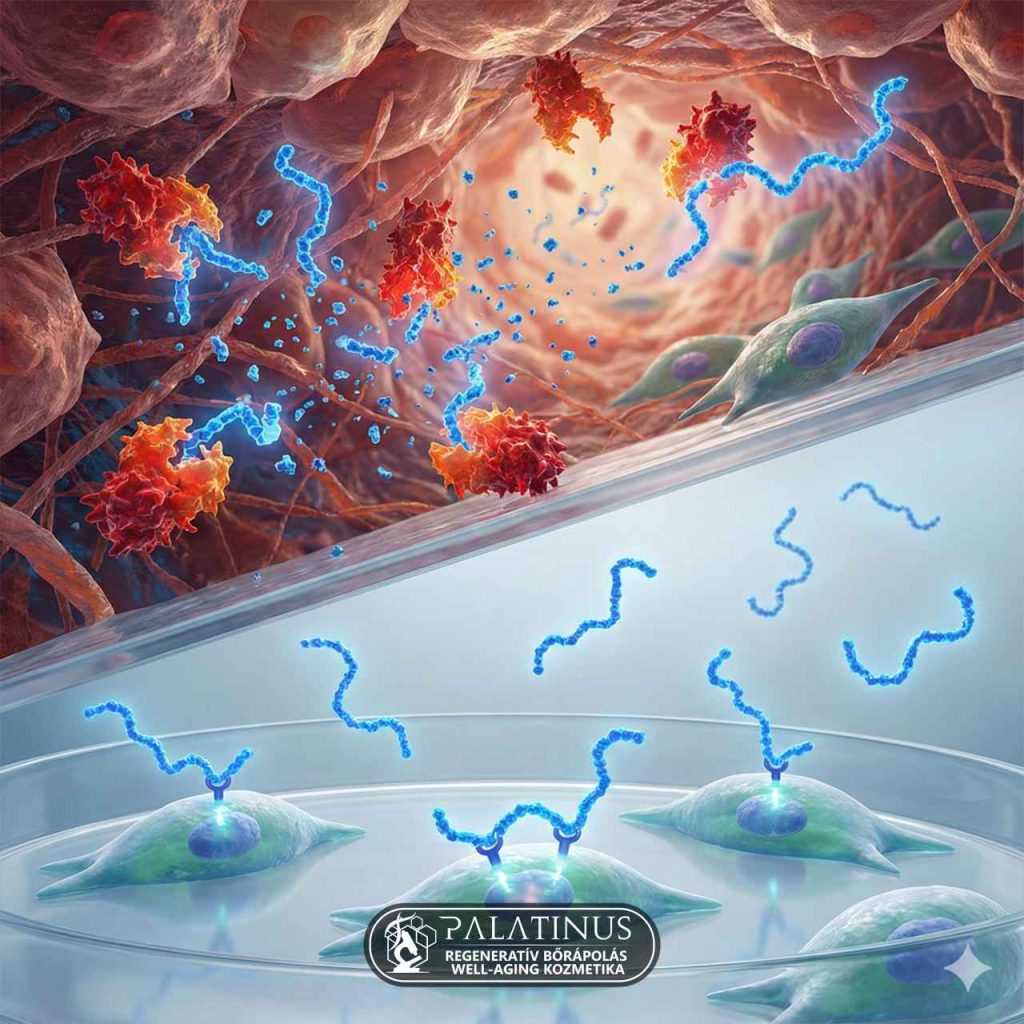
A probléma gyökere gyakran a kutatási módszertanban, a „Petricsésze-paradoxonban” keresendő. Levin és Momin (2010) átfogó tanulmánya rámutat, hogy a peptidek hatékonyságát igazoló kozmetikai alapanyag-tesztek jelentős része in vitro körülmények között születik. Ezekben a kísérletekben a molekulákat közvetlenül tenyésztett keratinocita vagy fibroblaszt sejtekre applikálják, steril, enzimmentes táptalajban. Ebben az idealizált környezetben hiányzik a stratum corneum fizikai akadálya, a bakteriális flóra és a degradáló enzimaktivitás, így a peptidek akadálytalanul kötődhetnek a receptorokhoz. Ez a modell azonban a biológiai potenciált méri, nem a klinikai realitást. Az élő emberi szövet (in vivo) ezzel szemben egy biokémiai akadálypálya, ahol a koncentráció-gradiens fenntartása a degradáció ellenében szinte lehetetlen feladat megfelelő védelem nélkül.
Következésképpen a dermatológiai farmakológia jelenlegi álláspontja, összhangban Jones és mtsai. (2013) vizsgálataival a palmitoilált peptidek penetrációjáról egyértelmű: a natív, módosítatlan peptidek topikális alkalmazása önmagában, fejlett vivőrendszerek (liposzómák, nanokapszulák) vagy kémiai stabilizálás (pl. acetilálás, palmitoilálás) nélkül statisztikailag elhanyagolható mértékű sejtkommunikációs választ vált ki a dermiszben. A molekulák túlnyomó többsége a felszíni barrier „enzim-darálójában” végzi, így bár a bőr hidratáltságát javíthatják, a mélyreható szerkezeti változásokért felelős szignáltranszdukció elmarad.
A folytatásban: A Proteolízis Árnyékában: A „Védtelen Peptidek” és a Bőr Barrierjének Kémiai Harca