Az Epidermális Csapda: A PDRN Biohasznosulásának Gátjai
Az előző fejezetben tisztáztuk, hogy a PDRN (polidezoxiribonukleotid) makromolekuláris mérete és polianionos töltése hogyan képez fizikai akadályt a passzív diffúzió előtt. De a tudományos analízis itt nem állhat meg. Feltételezve, hogy a molekula egy frakciója átjut a stratum corneum fizikai barrierjén, egy sokkal komplexebb kihívással kell szembenéznie: a bőr aktív biokémiai védelmi rendszerével.A bőrt ne…
Az előző fejezetben tisztáztuk, hogy a PDRN (polidezoxiribonukleotid) makromolekuláris mérete és polianionos töltése hogyan képez fizikai akadályt a passzív diffúzió előtt. De a tudományos analízis itt nem állhat meg. Feltételezve, hogy a molekula egy frakciója átjut a stratum corneum fizikai barrierjén, egy sokkal komplexebb kihívással kell szembenéznie: a bőr aktív biokémiai védelmi rendszerével.
A bőrt ne egy egyszerű, élettelen falként képzeljük el, hanem egy folyamatosan működő, intelligens védelmi rendszerként. Ha egy idegen hatóanyag (jelen esetben egy nukleinsav) bejut a sejtek közé, a bőr azonnal reagál, és elkezdi feldolgozni (processzálni) azt. Ez a feldolgozás három lépésben hiúsítja meg a hatóanyag mélyre jutását:
✧ először a bőr enzimjei darabokra vágják (enzimatikus degradáció),
✧ majd a felszíni sejtek a saját éhségük csillapítására elvonják az építőelemeket (metabolikus szekvesztráció),
✧ végül pedig a sejtek felszíni jelfogói egyszerűen magukhoz kötik a maradékot, így megakadályozva a továbbhaladást (receptor-mediált megkötés).
1. Enzimkatalitikus Degradáció (A Biokémiai Védvonal)
A PDRN biológiai hatásának elsődleges gátja az epidermiszben jelenlévő nukleáz aktivitás. A stratum corneum és a stratum granulosum határzónája gazdag extracelluláris enzimekben. Bőrgyógyászati szempontból kiemelkedő a DNáz II (savas endonukleáz) szerepe. Ennek aktivitási optimuma (pH 4.5–5.5) tökéletesen egybeesik a bőr fiziológiás savköpenyének kémhatásával.
A molekuláris következmény: Amikor a PDRN védelem nélkül kerül a bőrre, az endonukleázok hidrolizálják a polimer láncok foszfodiészter kötéseit. A biológiailag aktív, hosszú láncú polimerek gyorsan oligonukleotidokra, majd az extracelluláris enzimek (foszfatázok) révén egyszerű nukleozidokra hasadnak. A dermisz felé diffundáló anyag ekkor már nem a struktúraépítő PDRN, hanem egy kismolekulájú nukleotid/nukleozid elegy, amely elveszítette eredeti, specifikus biopolimer profilját.
2. A „Salvage Pathway” és a Metabolikus Szekvesztráció
A degradációt túlélő fragmentumok sorsa a metabolikus szekvesztráció (elvonás). A sejtek, különösen a gyorsan osztódó bazális keratinociták, rendelkeznek egy ún. nukleotid-mentőútvonallal (Salvage Pathway). Ez a mechanizmus lehetővé teszi, hogy a sejtek a környezetükből felvegyék a nukleozidokat saját DNS-replikációjukhoz, megspórolva a de novo szintézis energiáját.
✧ Epidermális „Éhség”: A stratum basale sejtjeinek nukleotid-igénye rendkívül magas.
✧ Transzport Mechanizmus: A keratinociták a felszínükön lévő specifikus transzportereken (pl. ENT1) keresztül aktívan felveszik a PDRN defoszforilált bomlástermékeit (nukleozidjait).
Ez farmakokinetikai szempontból „lopást” jelent: az epidermisz sejtjei metabolizálják a hatóanyag építőköveit, mielőtt azok elérhetnék a dermiszben lévő célsejteket, a fibroblasztokat.
3. Receptor Hierarchia: A Farmakodinámiás Paradoxon
Még ha a PDRN molekula intakt is maradna, szembe kell néznie a legkifinomultabb biológiai szűrővel: a receptor-kinetikával. A PDRN molekuláris célpontja az adenozin A2A receptor (A2AR). Shin és munkatársai (2023) friss kutatása rávilágított egy kritikus biológiai dualitásra: a PDRN hatása szigorúan sejtspecifikus.
A „Kétarcú” ERK-válasz:
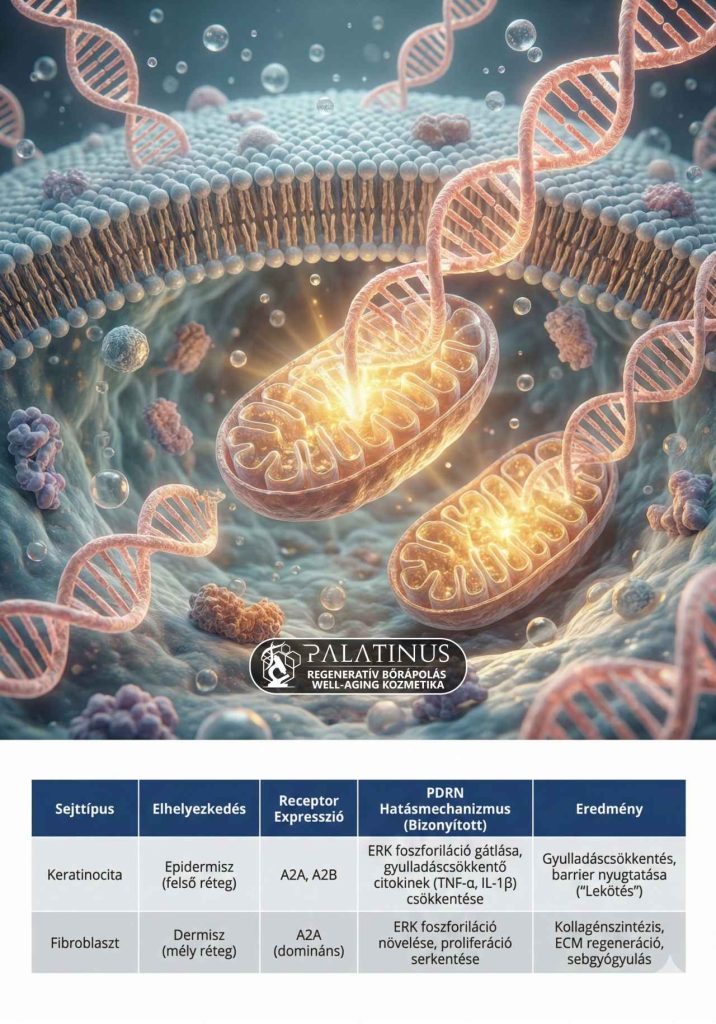
A kutatás az ERK (Extracellular Signal-Regulated Kinase) jelátviteli útvonal vizsgálatával igazolta, hogy ugyanaz a PDRN molekula ellentétes hatást vált ki a bőr két rétegében:
| Sejttípus | Réteg | PDRN hatása az ERK útvonalra | Kozmetológiai Eredmény |
| Keratinocita | Epidermisz (Felszín) | Gátlás (Down-regulation) | Gyulladásos citokinek (TNF-α, IL-6) csökkenése. |
| Fibroblaszt | Dermisz (Mély) | Aktiválás (Foszforiláció) | Proliferáció, kollagén (I, III) szintézis. Strukturális fiatalítás. |
Amikor a Célpont Visszalő: A TMDD Jelenség
A klasszikus kinetikában a koncentráció határozza meg, hány receptort tudunk aktiválni. A topikális alkalmazásnál azonban gyakran fordított a helyzet: a receptorok határozzák meg a hatóanyag sorsát. Ezt a jelenséget a tudomány Target-Mediated Drug Disposition (TMDD), azaz célpont-által közvetített hatóanyag-eloszlás néven ismeri.
Ha egy regeneráló formulát alkalmazunk, a hatóanyag először az epidermisz sűrű receptor-hálózatával találkozik. Mivel a PDRN nagy affinitással kötődik a felszíni purinerg (A2A) receptorokhoz, ezek a sejtek képesek „pufferelni” vagy „elkapkodni” a molekulákat. Ez jelentősen csökkenti a szabad hatóanyag mennyiségét, még mielőtt az elérhetné a dermisz célsejtjeit. Ez nem egyszerű felszívódási hiba, hanem egy kompetitív receptor-kötődési dinamika.
A Dermális „Sink Effect”: A Vérkeringés Paradoxona
Ha a hatóanyagnak sikerül is átjutnia a hámréteg „receptor-sorfalán” és nukleáz-védvonalán, a dermiszben egy újabb fizikai ellenséggel kell szembenéznie: a „Sink Effect”-tel (nyelő-hatás).
Míg az epidermisz érhálózatmentes, a dermisz gazdag kapilláris hálózattal rendelkezik. A vérkeringés folyamatos „tisztító” mechanizmusként (clearance) működik: amint egy molekula belép a dermiszbe, a keringés igyekszik elszállítani onnan a koncentráció-gradiens fenntartása érdekében.
Ez farmakokinetikai paradoxont szül a bőrápolásban: a hatóanyagnak bőrben tartott (kután) retencióra van szüksége a sejtregenerációhoz, miközben a keringés elszállításra törekszik. A cél tehát nem a hatóanyag „vérbe juttatása”, hanem a dermiszben való „lehorgonyzása”.
A Koncentráció Kritikus Szerepe: Dózisfüggő Válasz
A Shin-féle kutatás (2023) rámutatott, hogy a sejtek válasza szigorúan dózisfüggő. (Fontos megjegyezni, hogy ezek in vitro, sejtszinten mért célkoncentrációk, amelyeket egy egyszerű krém felszíni felkenésével a bőr mélyén szinte lehetetlen elérni a fent említett barrier-funkciók és a TMDD miatt.)
✧ Fibroblasztok: A kollagénszintézishez és az ERK aktiválásához magasabb, 10 µg/ml körüli sejtszintű koncentráció szükséges.
✧ Keratinociták: A bőrnyugtató hatáshoz elegendő az 1 µg/ml. Sőt, a túlzott felszíni koncentráció paradox módon gátolhatja a hámregenerációt, miközben a mélyben lévő fibroblasztok „éheznek”.

4. A Formulázási Tévedés: Biomimetikum vs. Enkapszuláció
A kozmetikai piacon gyakori tévhit a „bőrbarát” szerkezet és a „hatóanyag-védelem” összemosása. Tisztáznunk kell a kolloidkémiai realitást. Számos termék alkalmaz biomimetikus, lamelláris szerkezetű emulziókat. Bár ezek a lipidek kiválóan támogatják a barriert, a PDRN szempontjából nem nyújtanak védelmet. Mivel a PDRN vízoldékony (polianionos) makromolekula, az emulziókban kényszerűen a külső vizes fázisban oldódik, és nem záródik vezikulába. A molekulák nincsenek elzárva a környezettől, így felvitelkor azonnal érintkeznek a bontóenzimekkel. A „csupasz” PDRN topikális alkalmazása emiatt döntően csak felszíni hatást eredményez.
Konklúzió: Melyik bőrrétegig jut el „Segítség Nélkül”?
✧ Stratum Corneum: A hatóanyag döntő többsége itt marad, kiváló filmképző és vízmegkötő (hidratáló) hálót képezve.
✧ Epidermisz: A lebomlott, defoszforilált, kisebb molekulájú frakciók elérik a hámsejteket, ahol gátolják az ERK útvonalat, csökkentik a citokintermelést és a melanogenezist. Eredmény: kiváló bőrnyugtató és pigment-uniformizáló hatás.
✧ Dermisz (Fibroblasztok): Segítség nélkül a nagy molekulasúlyú PDRN nem képes biológiailag értékelhető koncentrációban átjutni a dermo-epidermális junkción (DEJ). A valódi kollagén-indukció nagy eséllyel elmarad.
Marketingmítoszok vs. Biokémiai Realitás
A kozmetikai ipar és a laikus véleményvezérek hajlamosak a végletekig leegyszerűsíteni a PDRN technológiát, és túlzó marketinggel értékesíteni azt, kihasználva a gyártók és a vásárlók közötti információs aszimmetriát.
Amikor egy hagyományos (nem nanovektoriális, egyszerű emulziós vagy gél bázisú) topikális PDRN krém leírásában a „mélyrétegi DNS-regeneráció”, a „szerkezeti fiatalodás”, vagy a „kollagén-indukciós sejtmegújítás” szlogeneket olvassuk, racionálisan tudnunk kell: megfelelő segédtechnológia (vektorálás) nélkül ez szigorú biokémiai és biofizikai korlátokba ütközik.
Ugyanakkor a tudományos objektivitás megköveteli, hogy tisztázzunk egy fontos tényt: a felszíni hatás nem egyenlő a hatástalansággal. Egyáltalán nem probléma (sőt, kifejezetten előnyös), ha egy topikális PDRN készítménytől „csak” felszíni hidratációt, ATP-szintézis támogatást és gyulladáscsökkentést kapunk. A bőr saját enzimjei által lebontott PDRN építőkövei (különösen az adenozin) igazoltan kiváló munkát végeznek az epidermiszben: csillapítják az irritációt és sejtenergiát (ATP) biztosítanak a hámsejteknek. A probléma tehát nem a hatóanyaggal van, hanem a túlzó, DNS-szintű fibroblaszt-aktivációt és kollagénstimulációt erőltető marketinggel, amelyet a helyén kell kezelnünk.
Két alapvető iparági csúsztatást kell tisztán látnunk:
✧ A „Magas Koncentráció” Illúziója: A gyártók gyakran licitálnak egymásra a PDRN százalékos arányával. Csakhogy a felszívódás törvényei nem így működnek. Ha a molekula mérete és töltése miatt eleve korlátozottan tud átjutni a barrieren, és a felszíni enzimek gyorsan hidrolizálják, akkor a koncentráció növelése csupán a felszínen rekedt építőelemek mennyiségét növeli. Ha egy elefántot akarunk átküldeni egy kulcslyukon, nem az a megoldás, hogy két elefántot tolunk oda. A dózis növelése soha nem helyettesíti a penetrációt.
✧ A Hatásmechanizmusok Szándékos Összemosása: A leginkább félrevezető reklámfogás (marketing manipuláció), amikor a reklámszövegek az orvosi, injekciós (vagy mikrotűs mezoterápiás) PDRN kutatások eredményeit (amelyek valóban bizonyítják a mélyrétegi fibroblaszt aktivációt és a heggyógyulást) szakmailag megalapozatlanul ráhúzzák a topikális, kenhető krémekre. Ez etikailag rendkívül aggályos csúsztatás. A két beviteli mód farmakokinetikája (ahogy a fentiekből is látszik) köszönőviszonyban sincs egymással. Egy prémium árazású krém, hiába tartalmazza ugyanazt a molekulát, tűs bejuttatás vagy intelligens nanovektorok nélkül sosem fog úgy viselkedni, mint egy orvosi injekció.Egy hatóanyag önmagában hiába jelent csodát a Petri-csészében vagy egy orvosi fecskendőben, ha a topikális formulációja elavult. Aki kiváló bőrnyugtatót és felületi hidratálót keres, annak a hagyományos PDRN krémek tökéletesek. De aki valódi, mélyrétegi sejtregenerációt és kollagén-indukciót vár, annak nem csupán a PDRN koncentrációit kell keresnie a dobozon, hanem a bejuttatás modern technológiáját is.
A Jövő Technológiái: A Vektoriális Szállítás
Hogyan juttathatjuk át sértetlenül ezt az értékes molekulát a „biológiai akadálypályán”?
✧ A megoldást a gyógyszertechnológiából átemelt nanovesikuláris rendszerek jelenthetik.
✧ A következő, záró fejezetben a modern hatóanyag-szállítás csúcsát, a Nanotechnológiás Vektorokat vesszük górcső alá.
✧ Megvizsgáljuk, hogyan képesek a Deformálható Liposzómák, az Etoszómák és a Polimer Nanoszómák „láthatatlanná” tenni a PDRN-t az enzimek számára, és precíziós bombaként eljuttatni azt közvetlenül a fibroblasztokhoz.
Források: (PMC5405115), (Impact), (PMC12473307), (PMC7559928) (Journals), (MDPI), (PMC8879610), (JIDonline), (PMC11172165), (PMC10308489), (PMC12785872), (Journals), (PubMed), (ScientificResearch), (Frontier), (PMC3046983), (PMC4505827), (RGate), (PMC7076422), (BJPS)